創新研發中心研發長林欣榮院長、副研發長韓鴻志教授、東華大學特聘教授邱紫文等人帶領的研發團隊,研究成果已連續六年獲國家新創獎學研新創獎肯定。
2019年,新藥創新研發團隊,發現標靶小分子藥物EF-001用於抑制癌症免疫檢查點PD-L1,使免疫T細胞活化,增強惡性膠質母細胞瘤免疫治療效果,是全球惡性腦瘤免疫治療研究大突破,榮獲國家新創獎「學研新創獎」。更早,用來治療惡性腦瘤的標靶新藥Cerebraca ® wafer ,已進入第二期臨床試驗。
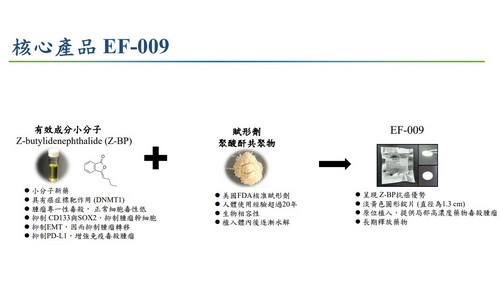
圖說:開發治療胰臟癌新藥EF-009 花蓮慈院獲國家新創獎。
韓鴻志教授表示,關於惡性腦瘤及胰臟癌的治療,在臨床醫學上是非常棘手的癌症,以胰臟癌來講,發生原因主要是胰臟透過「腫瘤基質纖維化」(desmoplastic stroma)形成纖維化保護層,阻礙化療藥物的攻擊,目前一般治療胰臟癌藥物,都很難滲透進去,治療後的結果不佳,存活中位數僅六至八個月,五年存活率僅5%,無法滿足醫療需求,臨床上仍然缺少有效的胰臟癌藥物。
相較於化療臨床用藥,Gemcitabine 在過去試驗中約延長胰臟癌動物模式約2週之壽命,韓鴻志教授說,新藥EF-009針對胰臟癌治療的動物試驗中,則能夠有效延長試驗動物約2.2倍壽命,後續還將開發進行偕同作用的口服藥。
韓鴻志教授指出,胰臟癌新藥EF-009,經內視鏡手術植入,貼在胰臟表面,利用局部藥物高濃度、高滲透、長時效的特性,慢慢釋放一個月,是穿透腫瘤基質纖維化保護牆後,抑制癌細胞的免疫檢查點PD-L1,也就是關掉癌細胞抑制免疫T細胞的「煞車」,活化T細胞後就可以辨認出腫瘤,進而殺死腫瘤細胞,提升免疫治療的效果。這是首款由臺灣研發、取得多國專利、並技轉廠商的胰臟癌藥物。
韓鴻志教授指出,EF-009標靶藥貼片植入胰臟治療一個月後,再接續典型治療,而且與口服TS-1有偕同作用,可持續抑制PD-L1,讓T細胞認出並殺死胰臟癌細胞;這項標靶治療目標則是鎖定基轉移酵素(DNA methyltransferase, DNMT)中的單磷酸腺苷活化蛋白質激酶(AMP activated protein kinase, AMPK)。
目前 EF-009的臨床前期開發已完成,除擁有符合PIC/S GMP國際標準原料藥、賦形劑、植入錠片製程外,EF-009在藥物毒性試驗、安全性藥理試驗、基因毒試驗、藥物動力學試驗等,亦有結果初步證實其安全性與藥物代謝特性。
這項新藥技術已轉移給長弘生技公司,並通過美國食藥署與臺灣衛福部的 IND (investigate new drug; 新藥臨床試驗許可),即將進入第一期臨床試驗,測試新藥用在人體的安全性及有效性,期許在未來能夠幫助需要治療的胰臟癌病人。
韓鴻志教授指出,創研團隊除了將著手進行後續新藥開發,新藥EF-009相關研究成果也將在12月2日至5日的台灣醫療科技展發表展出。
